Кюрий
Кюрий (лат. Curium; Cm) — Менделеевтің Периодтық кестесінің актинидтер тобындағы химиялық элемент.
| |||||||||||||||
| Атом қасиеті | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Атауы, символ, нөмірі |
Кюрий, 96 | ||||||||||||||
| Топ типі | |||||||||||||||
| Топ, период, блок |
III, 7, f | ||||||||||||||
| Атомдық масса (молярлық масса) | |||||||||||||||
| Электрондық конфигурация |
[Rn] 5f7 6d1 7s2 | ||||||||||||||
| Қабықшалар бойынша электрондар |
2, 8, 18, 32, 25, 9, 2 | ||||||||||||||
| Атом радиусы |
299; эмпирикалық: 174 пм | ||||||||||||||
| Химиялық қасиеттері | |||||||||||||||
| Ковалентті радиус |
169±3 пм | ||||||||||||||
| Электртерістілігі |
1,3 (Полинг шкаласы) | ||||||||||||||
| Электродты потенциал |
Cm←Cm3+ -2,06 В | ||||||||||||||
| Тотығу дәрежелері |
+3, +4, +5, +6 | ||||||||||||||
| Иондалу энергиясы (бірінші электрон) | |||||||||||||||
| Жай заттың термодинамикалық қасиеттері | |||||||||||||||
| Термодинамикалық фаза | |||||||||||||||
| Тығыздық (қ.ж.) |
13,51 г/см³ | ||||||||||||||
| Балқу температурасы |
1613 K | ||||||||||||||
| Қайнау температурасы |
3383 K | ||||||||||||||
| Молярлық жылусыйымдылық |
27 Дж/(K·моль) | ||||||||||||||
| Молярлық көлем | |||||||||||||||
| |||||||||||||||
| Жай заттың кристаллдық торы | |||||||||||||||
| Тор құрылымы |
Алтыбұрышты | ||||||||||||||
| Тор параметрлері |
a=3,496 c=11,33 Å | ||||||||||||||
| c/a қатынас |
3,24 | ||||||||||||||
| Басқа да қасиеттері | |||||||||||||||
| CAS нөмірі |
7440-51-9 | ||||||||||||||
Curium (Cm)
Рет нөмірі – 96.
Атомдық массасы – 247,0703.
Радиоактивтіктің негізін салушы Мария мен Пьер Кюрилердің құрметіне "Кюрий" деп атаған.
-
Мария Кюри, 1911
Кюрий табағатта кездеспейді. 1944 ж. американ ғылымы Г.Сиборг, Р.Джеймс және А.Гиорсо 239Pu Плутонийді α-бөлшектермен (гелий ионымен) атқылау арқылы жасанды түрде алған:
Кюрийдің 8 изотопы белгілі, бұлардың ішінде ең тұрақтысы 247Сm.
Физикалық қасиеттері
өңдеуКюрий - күміс түсті ақ металл.
Үшфторидті барий буымен тотықсыздандыру арқылы алынады.
Химиялық қасиеттері жағынан гадолинийге ұқсас.
Қосылыстарында үш валентті. Төрт валентті (СmО2,СmҒ4) қосылыстары кездеседі, бірақ тұрақсыз.
Тағы қараңыз
өңдеуСыртқы сілтемелер
өңдеу| Ортаққорда бұған қатысты медиа файлдар бар: Curium |
Дереккөздер
өңдеу- “Қазақстан”: Ұлттық энциклопедия/Бас редактор Ә. Нысанбаев – Алматы “Қазақ энциклопедиясы” Бас редакциясы, 1998

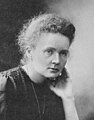

![{\displaystyle \mathrm {^{239}_{\ 94}Pu\ {\xrightarrow {2(n,\gamma )}}\ _{\ 94}^{241}Pu\ {\xrightarrow[{14,35\ a}]{\beta ^{-}}}\ _{\ 95}^{241}Am\ {\xrightarrow {(n,\gamma )}}\ _{\ 95}^{242}Am\ {\xrightarrow[{16,02\ h}]{\beta ^{-}}}\ _{\ 96}^{242}Cm} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/efd418dc9806641144fdbced4b2859e97d03d534)